适应症
非小细胞肺癌:
1、 联合治疗本品联合培美曲塞和卡铂用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌(NSCLC)患者的一线治疗。本品联合紫杉醇和卡铂用于转移性鳞状非小细胞肺癌(NSCLC)患者的一线治疗。
2、 单药治疗2本品用于在接受铂类药物为基础的同步或序贯放化疗后未出现疾病进展的、不可切除、III期非小细胞肺癌(NSCLC)患者的治疗。
用法用量
本品须在有肿瘤治疗经验的医生指导下用药。
推荐剂量
本品推荐剂量为1200 mg /次,静脉输注每3周给药1次,每次输注时间为60分钟或以上,直至出现疾病进展或产生不可耐受的毒性。如用于巩固治疗,本品治疗最长不超过24个月。根据个体患者的安全性和耐受性,可能需要暂停给药或永久停药。不建议增加或减少剂量。有关暂停给药和永久停药的指南,请见表1所述。有关免疫相关不良反应管理的详细指南,请参见【注意事项】
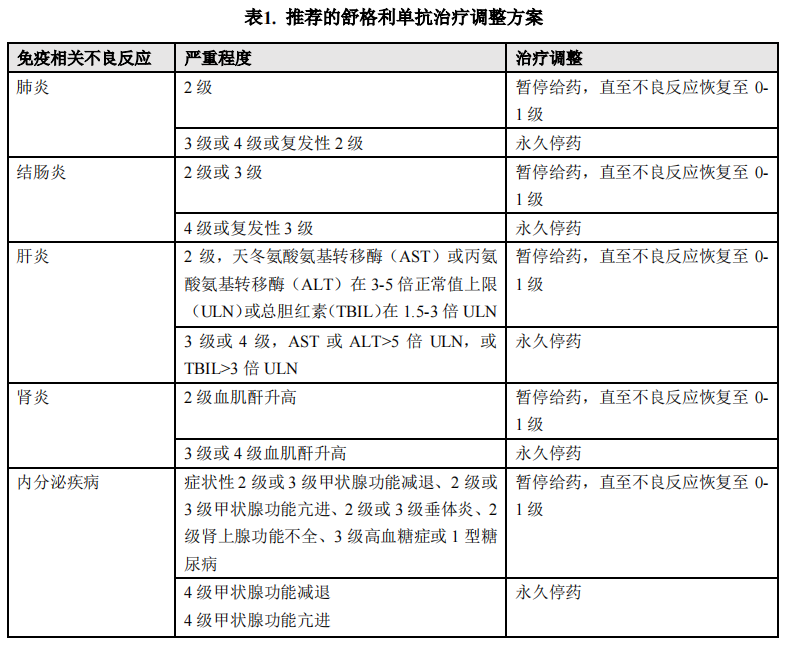
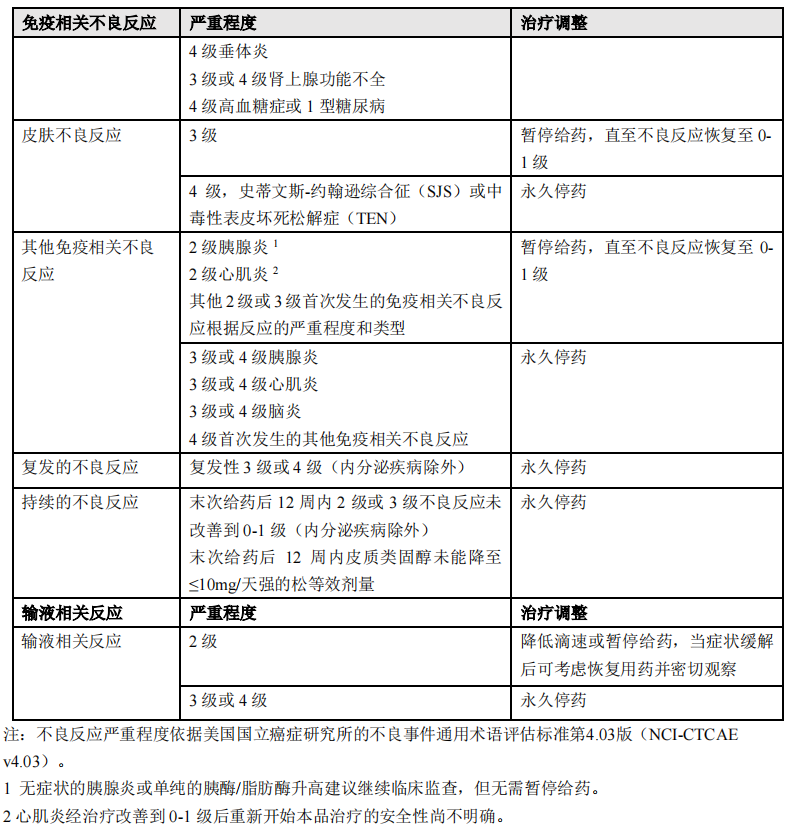
特殊人群
肝功能不全
目前本品尚无针对中重度肝功能不全患者的研究数据,中度或重度肝功能不全患者不推荐使用。轻度肝功能不全患者无需进行剂量调整。肾功能不全目前本品尚无针对重度肾功能不全患者的研究数据,重度肾功能不全患者不推荐使用。轻度或中度肾功能不全患者应在医生指导下慎用本品,基于群体药代动力学结果(参见【药代动力学】),如需使用,无需进行剂量调整。
儿童人群本品尚无在18岁以下儿童及青少年中的安全性和有效性数据。老年人群老年(≥65岁)与年轻患者(<65岁)在安全性或有效性上未出现总体的差异。无需在这一人群中进行剂量调整。
给药方法
本品应该由专业卫生人员采用无菌技术稀释后才可输注。本品须采用静脉输注的方式给药,输注应在60分钟或以上完成。
使用、处理、处置的特殊说明:
•禁止静脉内推注或快速注射(Bolus)。
•药物配置前确保药物溶液是澄清、透明、无肉眼可见微粒。
•以注射器抽取舒格利单抗注射液,注射液体积一共40mL(20mL/瓶:2瓶)。注入至250mL生理盐水(0.9%氯化钠溶液)静脉输液袋中。
•混合时轻轻颠倒混匀,禁止震摇。•输注时间应不低于60分钟,若出现1-2级输液反应,可暂停输液或适当延长输液时间,出现3级及以上输液反应立即停止输液并予以对症处理。
•请勿使用同一输液管与其他药物同时给药。
•建议药物应在配制完成后立即给予患者,以避免配制好的药物暴露于室温超过推荐的6小时限制。其中,6小时的时间限制包括药物室温贮存、静脉输液袋中输注液贮存和输注持续时间。如果需要推迟使用配制好的药物,则可将其置于2~8°C冰箱中,不超过24小时。
不良反应
接受舒格利单抗单药治疗的493例患者中所有级别的不良反应发生率为79.1%
最常见(发生率≥10%)的不良反应包括:贫血、丙氨酸氨基转移酶升高、天门冬氨酸氨基转移酶升高、甲状腺功能减退症、发热、肺部炎症、蛋白尿、皮疹、高血糖症。
3级及以上不良反应发生率为14.8%
其中发生率>1%的包括:贫血、肺部炎症、丙氨酸氨基转移酶升高、天门冬氨酸氨基转移酶升高、血胆红素升高、低钠血症、皮疹。
禁忌
对【成份】所列的活性成份或任何辅料存在超敏反应的患者。
贮存方法
本品在2~8℃避光保存与运输,不得冷冻
适用人群
不建议在妊娠期、哺乳期间使用;需避孕;
药物相互作用
舒格利单抗是一种全人源单克隆抗体,由于单克隆抗体不通过细胞色素CYP450酶或其他药物代谢酶代谢,也不主要以转运体介导的方式摄取和外排,所以合并使用对常见代谢酶或转运体的抑制或诱导作用预期不会影响本品的药代动力学特征。
因可能影响本品的药效学活性,应避免在开始本品治疗前使用全身性皮质类固醇及其他免疫抑制剂。如果为治疗免疫相关不良反应,可以在开始本品治疗后使用全身性皮质类固醇及其他免疫抑制剂(参见【注意事项】)。
有效期
24个月
剂型
注射剂
生产厂家
中国基石药业
成分
活性成份:舒格利单抗(全人源抗程序性死亡配体-1单克隆抗体)。
辅料:组氨酸、盐酸组氨酸、甘露醇、氯化钠、聚山梨酯80 (Ⅱ)。
性状
无色或淡黄色澄明液体,可带轻微乳光。
注意事项
免疫相关不良反应
接受本品治疗的患者可发生免疫相关不良反应,包括严重和致死病例。免疫相关不良反应可发生在本品治疗期间及停药以后,可能累及任何组织器官。对于疑似免疫相关不良反应,应进行充分的评估以确定病因或排除其他病因。大多数免疫相关不良反应是可逆的,并且可通过中断本品治疗、给予皮质类固醇治疗和/或支持治疗来处理。整体而言,对于大部分2级以及某些特定的3级和4级免疫相关不良反应需暂停给药。对于4级及某些特定的3级免疫相关不良反应需永久停药(参见【用法用量】)。对于3级和4级及某些特定的2级免疫相关不良反应,根据临床指征,给予1-2mg/kg/天强的松等效剂量及其他治疗,直至改善到≤1级。皮质类固醇需至少一个月的时间逐渐减量直至停药,快速减量可能引起不良反应恶化或复发。如果不良反应在皮质类固醇治疗后继续恶化或无改善,则应增加非皮质类固醇类别的免疫抑制剂治疗。本品给药后任何复发性3级或4级免疫相关不良反应(内分泌疾病除外),末次给药后12周内2级或3级免疫相关不良反应未改善到0-1级(内分泌疾病除外),以及末次给药后12周内皮质类固醇未能降至≤10mg/天强的松等效剂量,应永久停药。
免疫相关性肺炎
在接受本品治疗的患者中有免疫相关性肺炎的报告(参见【不良反应】)。应监测患者是否有肺炎症状和体征,如呼吸困难、缺氧表现、咳嗽、胸痛等,以及放射学改变(例如局部毛玻璃样混浊、斑块样浸润)。疑似免疫相关性肺炎的病例应采用影像学、肺功能、动脉血氧饱和度等检查进行评估和确认,并排除感染、疾病相关等其他病因。对于2级免疫相关性肺炎的患者,应暂停本品治疗。对于3级或4级或复发性2级免疫相关性肺炎,应永久停止本品治疗(参见【用法用量】)。
免疫相关性结肠炎
在接受本品治疗的患者中有免疫相关性结肠炎的报告(参见【不良反应】)。应监测患者是否有免疫相关性结肠炎相关症状和体征,如腹痛、腹泻、粘液便或血样便,并排除感染和基础疾病相关性病因。对于2级或3级免疫相关性腹泻或结肠炎,应暂停本品治疗。对于4级或复发性3级免疫相关性结肠炎,应永久停止本品治疗(参见【用法用量】)。应考虑肠穿孔的潜在风险,必要时行影像学和/或内镜检查以确认。
免疫相关性肝炎
在接受本品治疗的患者中有免疫相关性肝炎的报告(参见【不良反应】)。应定期(每个月)监测患者肝功能的变化及肝炎相应的症状和体征,并排除感染及与基础疾病相关的病因。如发生免疫相关性肝炎,应增加肝功能检测频率。给予皮质类固醇治疗[初始剂量为0.5-1 mg/kg/天(针对2级肝炎)和1-2 mg/kg/天(针对≥3级肝炎)泼尼松或等效剂量,之后逐渐减少剂量],并根据肝酶升高的严重程度决定是暂时停药还是永久停药。对于2级免疫相关性肝炎,应暂停本品治疗。对于3级或4级免疫相关性肝炎,应永久停止本品治疗(参见【用法用量】)。
免疫相关性肾炎
在接受本品治疗的患者中有免疫相关性肾炎报告(参见【不良反应】)。应定期(每个月)监测患者肾功能的变化及肾炎相应的症状和体征。如发生免疫相关性肾炎,应增加肾功能检测频率。多数出现血清肌酐升高的患者无临床症状。应排除肾功能损伤的其他病因。肾功能变化,排除肾功能损伤的其他病因。对于≥2级肾炎给予皮质类固醇(初始剂量为1-2 mg/kg/天泼尼松或等效剂量,之后逐渐减少剂量)。2级血肌酐升高应暂停本品治疗。3级或4级血肌酐升高应永久停止本品治疗(参见【用法用量】)。
免疫相关性心肌炎
在接受本品治疗的患者中有免疫相关性心肌炎的报告(参见【不良反应】)。应对心肌炎的症状和体征进行监测,对于疑似免疫相关性心肌炎,应进行充分的评估以确认病因或排除其他病因,并进行心肌酶谱等相关检查。发生2级心肌炎时,应暂停本品治疗,并给予皮质类固醇治疗,心肌炎恢复至0-1级后能否重新开始本品治疗的安全性尚不明确。发生3级或4级心肌炎时,应永久停止本品治疗,并给予皮质类固醇治疗。应密切监测心肌酶谱、心功能等(参见【用法用量】)。
免疫相关性肌炎
在接受本品治疗的患者中有免疫相关性肌炎的报告(参见【不良反应】)。对于疑似免疫相关性肌炎,应进行充分的评估以确认病因或排除其他病因。发生2-3级肌炎时,应暂停本品治疗至肌炎恢复至0-1级。发生4级肌炎时,应永久停止本品治疗,并给予皮质类固醇治疗(参见【用法用量】)。考虑监测肌酸激酶,必要时行肌活检等。
免疫相关性内分泌疾病
甲状腺疾病
在接受本品治疗的患者中有甲状腺功能紊乱的报告,包括甲状腺功能亢进,甲状腺功能减退,甲状腺炎(参见【不良反应】)。应密切监测患者甲状腺功能的变化及相应的症状和体征。对于症状性2级或3级甲状腺功能减退,应暂停本品治疗,并根据需要开始甲状腺激素替代治疗。对于症状性2级或3级甲状腺功能亢进,应暂停本品治疗,并根据需要给予β-受体阻滞剂、抗甲状腺药物治疗或糖皮质激素治疗。如果怀疑有甲状腺急性炎症,可考虑暂停本品治疗并给予皮质类固醇治疗。当甲状腺功能减退或甲状腺功能亢进的症状改善及甲状腺功能检查恢复,可根据临床需要重新开始本品治疗。对于4级甲状腺功能亢进或甲状腺功能减退,须永久停止本品治疗。应持续监测甲状腺功能,确保恰当的治疗(参见【用法用量】)。
垂体炎
接受本品治疗的患者中有垂体炎的报告(参见【不良反应】)。应对垂体炎患者的症状和体征进行监测(包括垂体功能减退和继发性肾上腺功能不全),并排除其他病因。监测和评估垂体相关的激素水平,必要时进行功能试验,考虑垂体MRI检查和自身免疫性抗体检查。发生症状性2级或3级垂体炎时应暂停本品治疗,并根据临床需要给予激素替代治疗。如果怀疑急性垂体炎,可给予皮质类固醇治疗。发生4级垂体炎时须永久停止本品治疗。应持续监测垂体功能、肾上腺功能和激素水平,根据临床指征给予皮质类固醇和其他激素替代疗法(参见【用法用量】)。
糖尿病
接受本品治疗的患者报告了高血糖症(参见【不良反应】)。应对患者的血糖水平或其他糖尿病症状和体征进行监测。根据临床需要给予胰岛素替代治疗。3级高血糖症或1型糖尿病患者,应暂停本品,给予胰岛素替代治疗直至症状缓解。对于4级高血糖症或1型糖尿病患者,须永久停用本品。应持续监测血糖水平,确保适当的胰岛素替代治疗(参见【用法用量】)。免疫相关性皮肤不良反应在接受本品治疗的患者中有免疫相关性皮肤不良反应的报告(参见【不良反应】)。应监测患者的重度皮肤不良反应,并应排除其他病因。对于1级或2级皮疹,可继续本品治疗,并对症治疗或进行局部皮质类固醇治疗。发生3级皮疹时应暂停本品治疗,并对症治疗或进行局部皮质类固醇治疗。发生4级皮疹、确诊SJS或TEN时应永久停止本品治疗(参见【用法用量】)。
其他免疫相关不良反应
在本品临床试验中,还在小于1%的患者中报告了包括胰腺炎、全血细胞减少/双系血细胞减少、溶血性贫血、关节炎、上消化道疾病的免疫相关不良反应(参见【不良反应】)。
本品须在有肿瘤治疗经验的医生指导下用药。
推荐剂量
本品推荐剂量为1200 mg /次,静脉输注每3周给药1次,每次输注时间为60分钟或以上,直至出现疾病进展或产生不可耐受的毒性。如用于巩固治疗,本品治疗最长不超过24个月。根据个体患者的安全性和耐受性,可能需要暂停给药或永久停药。不建议增加或减少剂量。有关暂停给药和永久停药的指南,请见表1所述。有关免疫相关不良反应管理的详细指南,请参见【注意事项】


特殊人群
肝功能不全
目前本品尚无针对中重度肝功能不全患者的研究数据,中度或重度肝功能不全患者不推荐使用。轻度肝功能不全患者无需进行剂量调整。肾功能不全目前本品尚无针对重度肾功能不全患者的研究数据,重度肾功能不全患者不推荐使用。轻度或中度肾功能不全患者应在医生指导下慎用本品,基于群体药代动力学结果(参见【药代动力学】),如需使用,无需进行剂量调整。
儿童人群本品尚无在18岁以下儿童及青少年中的安全性和有效性数据。老年人群老年(≥65岁)与年轻患者(<65岁)在安全性或有效性上未出现总体的差异。无需在这一人群中进行剂量调整。
给药方法
本品应该由专业卫生人员采用无菌技术稀释后才可输注。本品须采用静脉输注的方式给药,输注应在60分钟或以上完成。
使用、处理、处置的特殊说明:
•禁止静脉内推注或快速注射(Bolus)。
•药物配置前确保药物溶液是澄清、透明、无肉眼可见微粒。
•以注射器抽取舒格利单抗注射液,注射液体积一共40mL(20mL/瓶:2瓶)。注入至250mL生理盐水(0.9%氯化钠溶液)静脉输液袋中。
•混合时轻轻颠倒混匀,禁止震摇。•输注时间应不低于60分钟,若出现1-2级输液反应,可暂停输液或适当延长输液时间,出现3级及以上输液反应立即停止输液并予以对症处理。
•请勿使用同一输液管与其他药物同时给药。
•建议药物应在配制完成后立即给予患者,以避免配制好的药物暴露于室温超过推荐的6小时限制。其中,6小时的时间限制包括药物室温贮存、静脉输液袋中输注液贮存和输注持续时间。如果需要推迟使用配制好的药物,则可将其置于2~8°C冰箱中,不超过24小时。
免疫相关不良反应
接受本品治疗的患者可发生免疫相关不良反应,包括严重和致死病例。免疫相关不良反应可发生在本品治疗期间及停药以后,可能累及任何组织器官。对于疑似免疫相关不良反应,应进行充分的评估以确定病因或排除其他病因。大多数免疫相关不良反应是可逆的,并且可通过中断本品治疗、给予皮质类固醇治疗和/或支持治疗来处理。整体而言,对于大部分2级以及某些特定的3级和4级免疫相关不良反应需暂停给药。对于4级及某些特定的3级免疫相关不良反应需永久停药(参见【用法用量】)。对于3级和4级及某些特定的2级免疫相关不良反应,根据临床指征,给予1-2mg/kg/天强的松等效剂量及其他治疗,直至改善到≤1级。皮质类固醇需至少一个月的时间逐渐减量直至停药,快速减量可能引起不良反应恶化或复发。如果不良反应在皮质类固醇治疗后继续恶化或无改善,则应增加非皮质类固醇类别的免疫抑制剂治疗。本品给药后任何复发性3级或4级免疫相关不良反应(内分泌疾病除外),末次给药后12周内2级或3级免疫相关不良反应未改善到0-1级(内分泌疾病除外),以及末次给药后12周内皮质类固醇未能降至≤10mg/天强的松等效剂量,应永久停药。
免疫相关性肺炎
在接受本品治疗的患者中有免疫相关性肺炎的报告(参见【不良反应】)。应监测患者是否有肺炎症状和体征,如呼吸困难、缺氧表现、咳嗽、胸痛等,以及放射学改变(例如局部毛玻璃样混浊、斑块样浸润)。疑似免疫相关性肺炎的病例应采用影像学、肺功能、动脉血氧饱和度等检查进行评估和确认,并排除感染、疾病相关等其他病因。对于2级免疫相关性肺炎的患者,应暂停本品治疗。对于3级或4级或复发性2级免疫相关性肺炎,应永久停止本品治疗(参见【用法用量】)。
免疫相关性结肠炎
在接受本品治疗的患者中有免疫相关性结肠炎的报告(参见【不良反应】)。应监测患者是否有免疫相关性结肠炎相关症状和体征,如腹痛、腹泻、粘液便或血样便,并排除感染和基础疾病相关性病因。对于2级或3级免疫相关性腹泻或结肠炎,应暂停本品治疗。对于4级或复发性3级免疫相关性结肠炎,应永久停止本品治疗(参见【用法用量】)。应考虑肠穿孔的潜在风险,必要时行影像学和/或内镜检查以确认。
免疫相关性肝炎
在接受本品治疗的患者中有免疫相关性肝炎的报告(参见【不良反应】)。应定期(每个月)监测患者肝功能的变化及肝炎相应的症状和体征,并排除感染及与基础疾病相关的病因。如发生免疫相关性肝炎,应增加肝功能检测频率。给予皮质类固醇治疗[初始剂量为0.5-1 mg/kg/天(针对2级肝炎)和1-2 mg/kg/天(针对≥3级肝炎)泼尼松或等效剂量,之后逐渐减少剂量],并根据肝酶升高的严重程度决定是暂时停药还是永久停药。对于2级免疫相关性肝炎,应暂停本品治疗。对于3级或4级免疫相关性肝炎,应永久停止本品治疗(参见【用法用量】)。
免疫相关性肾炎
在接受本品治疗的患者中有免疫相关性肾炎报告(参见【不良反应】)。应定期(每个月)监测患者肾功能的变化及肾炎相应的症状和体征。如发生免疫相关性肾炎,应增加肾功能检测频率。多数出现血清肌酐升高的患者无临床症状。应排除肾功能损伤的其他病因。肾功能变化,排除肾功能损伤的其他病因。对于≥2级肾炎给予皮质类固醇(初始剂量为1-2 mg/kg/天泼尼松或等效剂量,之后逐渐减少剂量)。2级血肌酐升高应暂停本品治疗。3级或4级血肌酐升高应永久停止本品治疗(参见【用法用量】)。
免疫相关性心肌炎
在接受本品治疗的患者中有免疫相关性心肌炎的报告(参见【不良反应】)。应对心肌炎的症状和体征进行监测,对于疑似免疫相关性心肌炎,应进行充分的评估以确认病因或排除其他病因,并进行心肌酶谱等相关检查。发生2级心肌炎时,应暂停本品治疗,并给予皮质类固醇治疗,心肌炎恢复至0-1级后能否重新开始本品治疗的安全性尚不明确。发生3级或4级心肌炎时,应永久停止本品治疗,并给予皮质类固醇治疗。应密切监测心肌酶谱、心功能等(参见【用法用量】)。
免疫相关性肌炎
在接受本品治疗的患者中有免疫相关性肌炎的报告(参见【不良反应】)。对于疑似免疫相关性肌炎,应进行充分的评估以确认病因或排除其他病因。发生2-3级肌炎时,应暂停本品治疗至肌炎恢复至0-1级。发生4级肌炎时,应永久停止本品治疗,并给予皮质类固醇治疗(参见【用法用量】)。考虑监测肌酸激酶,必要时行肌活检等。
免疫相关性内分泌疾病
甲状腺疾病
在接受本品治疗的患者中有甲状腺功能紊乱的报告,包括甲状腺功能亢进,甲状腺功能减退,甲状腺炎(参见【不良反应】)。应密切监测患者甲状腺功能的变化及相应的症状和体征。对于症状性2级或3级甲状腺功能减退,应暂停本品治疗,并根据需要开始甲状腺激素替代治疗。对于症状性2级或3级甲状腺功能亢进,应暂停本品治疗,并根据需要给予β-受体阻滞剂、抗甲状腺药物治疗或糖皮质激素治疗。如果怀疑有甲状腺急性炎症,可考虑暂停本品治疗并给予皮质类固醇治疗。当甲状腺功能减退或甲状腺功能亢进的症状改善及甲状腺功能检查恢复,可根据临床需要重新开始本品治疗。对于4级甲状腺功能亢进或甲状腺功能减退,须永久停止本品治疗。应持续监测甲状腺功能,确保恰当的治疗(参见【用法用量】)。
垂体炎
接受本品治疗的患者中有垂体炎的报告(参见【不良反应】)。应对垂体炎患者的症状和体征进行监测(包括垂体功能减退和继发性肾上腺功能不全),并排除其他病因。监测和评估垂体相关的激素水平,必要时进行功能试验,考虑垂体MRI检查和自身免疫性抗体检查。发生症状性2级或3级垂体炎时应暂停本品治疗,并根据临床需要给予激素替代治疗。如果怀疑急性垂体炎,可给予皮质类固醇治疗。发生4级垂体炎时须永久停止本品治疗。应持续监测垂体功能、肾上腺功能和激素水平,根据临床指征给予皮质类固醇和其他激素替代疗法(参见【用法用量】)。
糖尿病
接受本品治疗的患者报告了高血糖症(参见【不良反应】)。应对患者的血糖水平或其他糖尿病症状和体征进行监测。根据临床需要给予胰岛素替代治疗。3级高血糖症或1型糖尿病患者,应暂停本品,给予胰岛素替代治疗直至症状缓解。对于4级高血糖症或1型糖尿病患者,须永久停用本品。应持续监测血糖水平,确保适当的胰岛素替代治疗(参见【用法用量】)。免疫相关性皮肤不良反应在接受本品治疗的患者中有免疫相关性皮肤不良反应的报告(参见【不良反应】)。应监测患者的重度皮肤不良反应,并应排除其他病因。对于1级或2级皮疹,可继续本品治疗,并对症治疗或进行局部皮质类固醇治疗。发生3级皮疹时应暂停本品治疗,并对症治疗或进行局部皮质类固醇治疗。发生4级皮疹、确诊SJS或TEN时应永久停止本品治疗(参见【用法用量】)。
其他免疫相关不良反应
在本品临床试验中,还在小于1%的患者中报告了包括胰腺炎、全血细胞减少/双系血细胞减少、溶血性贫血、关节炎、上消化道疾病的免疫相关不良反应(参见【不良反应】)。
 全部分类
全部分类





 舒格利单抗 Sugemalimab Cejemly
舒格利单抗 Sugemalimab Cejemly 中国基石药业
中国基石药业 用法用量
用法用量
