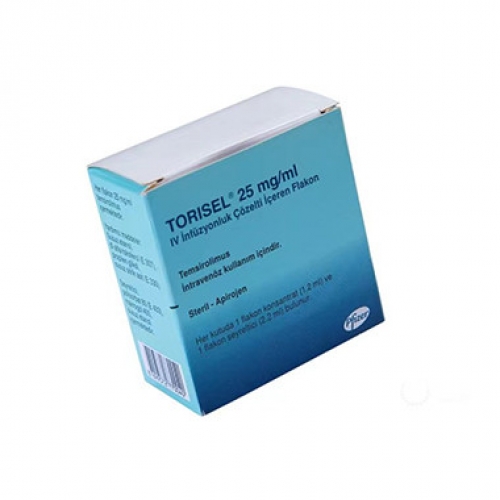
坦罗莫司(Temsirolimus)是一种用于治疗肾细胞癌的药物。那么,坦罗莫司是否已经获得中国食品和药品监督管理局(CFDA)的批准呢?让我们来看一看。
坦罗莫司药物在中国CFDA是否得到批准?
坦罗莫司(Temsirolimus)是一种口服抗肿瘤药物,用于治疗晚期肾细胞癌。它作用于肿瘤细胞内的信号途径,抑制细胞的生长和分裂。 这一药物在其它国家已经得到批准,并被广泛应用于肾细胞癌的治疗。但我们关注的是,它是否已经获得了中国食品和药品监督管理局(CFDA)的批准呢?下面,我们将逐一进行探讨。
1. CFDA:中国食品和药品监督管理局
中国食品和药品监督管理局(China Food and Drug Administration,简称CFDA)是中国负责监督药品和食品安全的官方机构。它的职责包括审批药品的上市,确保药品的质量、安全和疗效符合相关标准。
2. 坦罗莫司在中国的批准情况
目前,坦罗莫司在中国尚未获得中国食品和药品监督管理局(CFDA)的批准。这意味着坦罗莫司尚不具备在中国市场销售和使用的资格。
3. 临床研究和批准流程
要获得CFDA的批准,药物需要经历一系列严格的临床研究和审批流程。首先,药物开发者会在中国进行临床试验,验证药物的安全性和疗效。然后,药物开发者可以提交申请,要求CFDA对药物进行审批。CFDA会评估临床数据、药物质量和生产工艺等方面的信息,来决定是否批准该药物上市。
4. 坦罗莫司的前景
尽管坦罗莫司在中国尚未获得CFDA的批准,但并不意味着它没有治疗肾细胞癌的潜力。研究人员和医生仍然可以在合适的临床试验框架内使用坦罗莫司,以探索其在中国患者中的疗效和安全性。此外,药物的开发者也可以继续推进申请流程,争取在将来获得CFDA的批准,以使该药物能够在中国患者中普及使用。
截至目前,坦罗莫司(Temsirolimus)尚未获得中国食品和药品监督管理局(CFDA)的批准。这并不妨碍该药物在合适的临床试验中被研究和使用,以期望为中国的肾细胞癌患者提供新的治疗选择。无论如何,我们仍然需要关注药物审批流程的进展,以及它在中国市场的未来发展与应用。

 全部分类
全部分类

 美国辉瑞
美国辉瑞
 孟加拉耀品国际
孟加拉耀品国际
 孟加拉珠峰制药
孟加拉珠峰制药

 孟加拉碧康制药
孟加拉碧康制药
 美国AVEO
美国AVEO